Cellule 'invisibili' al sistema immunitario: chiave per il trapianto non compatibile?
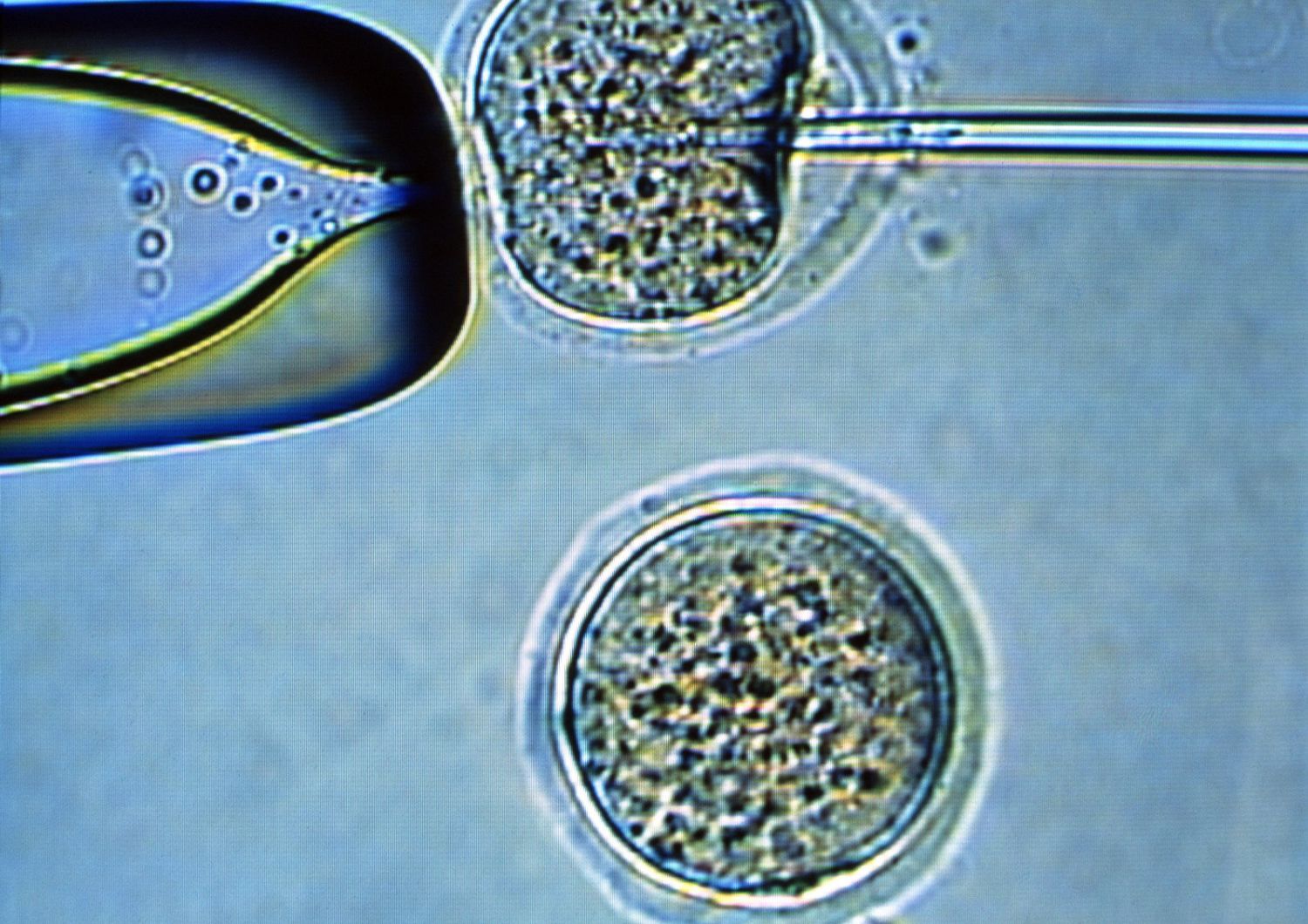

Nel 2009 la rivista scientifica Nature Methods definì metodo dell’anno la tecnica di laboratorio per ottenere cellule staminali da cellule adulte specializzate e in grado quindi di ritornare “bambine” per poi essere a loro volta indirizzate a diventare fegato, polmone, ossa, cuore, e qualunque altro tipo di tessuti. Il metodo ha permesso a Shinya Yamanaka di vincere il Premio Nobel nel 2012.
Queste cellule furono da lui definite iPS (cellule staminali pluripotenti indotte) perché indotte a perdere la loro specializzazione ed essere riprogrammate mediante tecniche di ingegneria genetica, aprendo di fatto la strada a nuove possibilità terapeutiche (la terapia cellulare), soprattutto nel settore dei trapianti di organo.
La terapia cellulare consiste nell’inserimento di cellule capaci di differenziare in tipi e sottotipi diversi all’interno di specifici tessuti o organi bersaglio, contribuendo così a ripristinare funzioni perse o danneggiate dei tessuti; le cellule iPS possono essere autologhe (ricevente e donatore sono la stessa persona), allogeniche (il donatore e il ricevente sono due persone diverse) e xenogeniche (le cellule del donatore provengono da animale).
Le cellule iPS autologhe hanno il vantaggio di eludere i problemi di rigetto nell’ospite e non incorrono nei limiti etici che vietano l’uso di cellule staminali embrionali. Ma hanno la grande limitazione di non poter essere utilizzate per un paziente affetto da una malattia genetica (la mutazione a meno che non venga riparata, rimane nelle cellule iPS).
Sarebbe bello, pertanto, utilizzare iPS da soggetti sani (donatori) un po’ come avviene oggi nei trapianti, ma sappiamo bene che proprio il rigetto da non-compatibilità costituisce il grande limite dei trapianti. Le iPS allogeniche e quelle xenogeniche, non sono utilizzabili quindi a fini terapeutici, perché provenendo da soggetti diversi (umani o animali) inducono forti reazioni immunogeniche.
Questa grande limitazione è stata oggi superata da un gruppo di ricercatori americani che sono stati in grado di generare cellule iPS “ipoimmunogeniche”, cioè cellule con ridotta o assente capacità di indurre rigetto nell’ospite una volta trasferite. È un grande risultato della ricerca ottenuto attraverso l’osservazione e la conoscenza di un fenomeno biologico noto da tempo: il mancato rigetto di un feto dal sistema immunitario materno. Durante la gravidanza infatti, il sistema immunitario materno è tollerante per gli antigeni paterni allogenici.
I ricercatori hanno scoperto che questo fenomeno è dovuto ad una ridotta espressione di certi geni MHC (i geni del sistema di istocompatibilità che permette di riconoscere il proprio dal non-proprio), e da una forte espressione del gene CD47, una proteina di membrana ubiquitaria che può interagire con diverse cellule recettori di superficie per inibire la fagocitosi (capacità delle cellule di ingerire materiali estranei e di distruggerli). Hanno quindi modificato geneticamente le cellule iPS modulando proprio i geni MHC e CD47.
Le cellule iPS così modificate non sono in grado di stimolare la risposta immune dell’ospite.
Un passo avanti nella ricerca sulle staminali, ma ancora pieno di interrogativi. Primo, le tecniche di riprogrammazione non sono ancora del tutto ottimizzate, per cui le mutazioni che potrebbero insorgere durante la riprogrammazione possono limitare la loro applicabilità e nello stesso tempo ridurre le loro capacità differenziative; secondo, queste cellule “invisibili” al sistema immunitario potrebbero un domani trasformarsi in tumorali perché non vengono riconosciute e quindi eliminate dal sistema immunitario? Terzo, i troppi interventi di “chirurgia genetica” non alterano le caratteristiche biologiche di queste cellule?
Nonostante queste considerazioni, che meritano certamente ulteriori approfondimenti, ritengo comunque che questo risultato potrebbe fornire un utile modello di studio per sviluppare in vitro modelli di malattie umane utili per capire ulteriormente le basi biochimiche dell’immunità e fornire indicazioni per terapie immunologiche in malattie come il lupus, la sclerosi multipla, il diabete e numerose altre patologie dell’autoimmunità.
Le iPS derivate da pazienti forniscono inoltre una libreria di tessuti per la validazione di terapie in vivo individuo-specifiche sia farmacologiche che di terapia genica, eliminando così il rischio tossicologico di trattamenti sull’individuo. Il processo di caratterizzazione di nuove sostanze farmacologiche è lungo e dispendioso, una gran quantità di composti che hanno passato il test sugli animali in realtà falliscono gli stadi successivi per motivi di efficacia e sicurezza, e quando vengono testati sull’uomo forniscono risultati incerti nei trials clinici.
In questo caso le iPSC mostrano diversi vantaggi: forniscono informazioni su come i farmaci agiscono sulle cellule umane, permettono uno screening su larga scala, mostrano una maggiore sensibilità e accuratezza, ed economicamente consentono un investimento più contenuto.
La scoperta delle iPSC ha aperto una nuova era e acceso molto entusiasmo. Queste cellule si sono imposte come sistema di studio per la patogenesi delle malattie, per la scoperta di nuovi farmaci e per i loro studi tossicologici, per protocolli di terapia cellulare. Le iPS derivate da pazienti forniscono poi una piattaforma unica per studiare in vitro le malattie umane e in particolare quelle legate a disordini dello sviluppo.
Nei prossimi anni, è probabile che molte terapie basate sulle cellule staminali saranno sperimentate in trial-clinici, rappresentando una soluzione promettente per il trattamento di tutte le malattie finora incurabili. La speranza è che in futuro, terapie cellulari personalizzate basate sulla somministrazione delle proprie cellule entreranno nella pratica clinica di ogni giorno.